- Labor
- Labormedizin
- Albumin-Reagenz
- MP Biomedicals
Protein-Reagenzkit 0718910-CFAntikörperAlbuminDiagnose
Zu meinen Favoriten hinzufügen
Zum Produktvergleich hinzufügen
Eigenschaften
- Typ
- Antikörper, Albumin
- Anwendung
- Diagnose
- Getesteter Marker
- Protein, Testosteron
Beschreibung
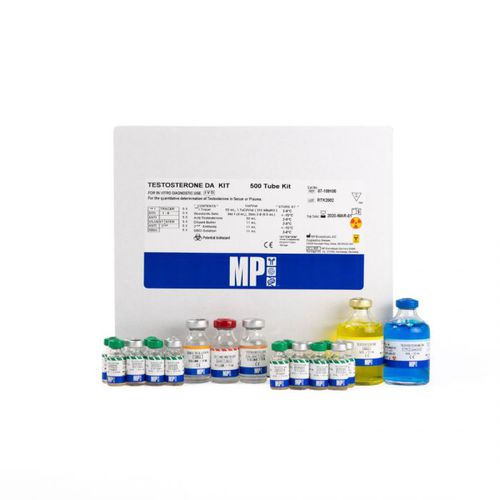
Der Testosteron-Doppelantikörper-RIA-Kit ist für den Nachweis und die Messung der gesamten unkonjugierten Form dieses Steroids bestimmt. Er unterscheidet nicht zwischen an Proteine (Albumin und SHBG) gebundenem Testosteron und echtem freien Testosteron, das nach einem Dialyseverfahren gemessen werden muss.
Erklärung zur Verwendung
FDA-Zulassung für die Verwendung als In-vitro-Diagnostikum (IVD) in den Vereinigten Staaten. CE-Kennzeichnung für IVD-Verwendung außerhalb der Vereinigten Staaten.
Analyte / Ziel - Testosteron
Basis-Katalognummer - 189101
Diagnostische Plattformen - RIA
Diagnostische Lösungen - Endokrinologie
Untersuchte Krankheit - Testosteron
Auswertung - Quantitativ
Probentyp - Plasma, Serum
Probenvolumen - 50 ul
Spezies Reaktivität - Mensch
Gebrauchsanweisung - FDA-Zulassung für die Verwendung als In-vitro-Diagnostikum (IVD) in den Vereinigten Staaten. CE-gekennzeichnet für IVD-Verwendung außerhalb der Vereinigten Staaten.
---
Kataloge
Für dieses Produkt ist kein Katalog verfügbar.
Alle Kataloge von MP Biomedicals anzeigenVerwandte Suchbegriffe
- Reagenzkit
- Testkit
- Reagenzkit / als Lösung
- Blut-Testkit
- Reagenzkit für Molekularbiologie
- Serum-Testkit
- Immunoassay-Testkit
- Flüssiges Reagenzkit
- Plasma-Testkit
- Reagenzkit für Forschungszwecke
- Testkit für Infektionskrankheiten
- Blutschnelltest
- Protein-Reagenzkit
- Diagnose-Reagenzkit
- Labor-Reagenzkit
- Lateral-Flow-Schnelltest
- Enzyme-Reagenzkit
- Immunologischer Schnelltest
- Molekularer Testkit
- Kassetten-Schnelltest
* Die Preise verstehen sich ohne MwSt., Versandkosten und Zollgebühren. Eventuelle Zusatzkosten für Installation oder Inbetriebnahme sind nicht enthalten. Es handelt sich um unverbindliche Preisangaben, die je nach Land, Kurs der Rohstoffe und Wechselkurs schwanken können.